Конспект уроку: Оксиген. Кисень, склад його молекули, фізичні властивості. Відкриття кисню
ознайомити з головними особливостями хімічного елементу Оксигену й його простою речовиною – Киснем;
визначити його склад та склад молекули;
описати фізичні властивості речовини та озайомитися із історією відкриття кисню.
Оксиген та Кисень, склад його молекули
Хімічним символом елемента Оксигену являється O.
У Оксигену відносна атомна маса Ar (О) = 16
Хімічною формулою простої речовини кисню є O2.
Відносна молекулярна маса кисню — Mr (O2) = 32.
Молярна маса — M(O2) = 32 г/моль.
Валентність Оксигену в різних сполуках дорівнює 2.
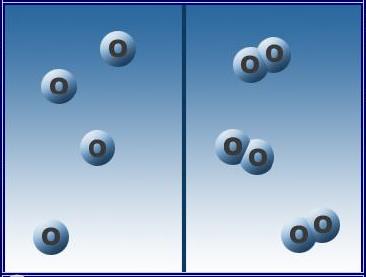
Рис. 1. Атом Оксигену і молекула кисню
Відкриття кисню
Належить пріоритет у відкритті кисню Китаю. Саме китайський вчений Мао–Хоа ще VIII ст. установив наявність в повітрі 2 газів, із яких один мав здатність підтримувати дихання та горіння.
У стародавній Європі кисень відкрили одночасно через 1000 років два видатних хіміка другої пол. XVIII ст. – шведський Карл Шеєле (1771 р.) та англійський Джозеф Прістлі (1774 р.). Однак К. Шеєле опублікував відкриття дещо пізніше, ніж Дж. Прістлі. Після цього на одному із майданів в місті Лідс вдячні англійці установили бронзову скульптуру видатного співвітчизника.

Рис. 2. Карл Вільгельм Шееле (1742 -1786).
Шведський хімік, чудовий експериментатор. Першим добув такі неорганічні речовини, як кисень, хлор, калій перманганат, манган, флуороводень та багато інших. Виділив та описав понад половину відомих у XVIII ст. органічних сполук. Довів багатокомпонентний склад повітря. Досліджував мінерали.

Рис. 3. Джозеф Прістлі (1733 - 1804).
Англійський хімік, філософ. Почесний член Петербурзької Академії наук (з 1780). Заклав основи науки про гази. Створив ряд приладів для вивчення газів. Відкрив кисень (1774), добув хлороводень і амоніак. Довів, що зелені рослини “виправляють" повітря, зіпсоване диханням і горінням. Відстоював теорію флогістону.
Однак головні особи у історії відкриття кисню ніяк не К. Шеєле та Дж. Прістлі. Справді вони відкрили новий газ, яким був кисень, однак до кінця власних днів залишалися захисниками помилкової теорії флогістону.
За хибним уявленнями вчених XVIII ст. флогістон – “вогняна матерія” - невагома речовина, котра ніби міститься у всіх речовинах, які здатні горіти, та котра під час горіння звітрюється й зникає.
У історії відкриття кисню значне значення мають роботи французького ученого Антуана Лавуазьє, який в 1775 р. встановив те, що кисень – це складова повітря, в свою чергу входить Оксиген до складу кислот й інших речовин.

Рис. Антуан Лоран Лавуазье (1743-1794).
Французький хімік, один із засновників сучасної хімічної науки. Систематично використовував у хімічних дослідженнях кількісні методи. Експерементально довів склад повітря, запропонував назву “кисень" і з’ясував роль кисню у процесах горіння, випалювання металів і дихання, чим спростував теорію флогістону. Один із засновників термохімії Керував розробкою нової хімічної номенклатури. Розробив систематику органічних сполук.
Саме А. Лавуазьє першим дослідив кисень й утворив кисневу теорію горіння, котра прийшла на заміну теорії флогістону. В період, який минув із того часу, киснева теорія горіння дістала іще безліч підтверджень власної правильності.
Фізичні властивості
Кисень за стандартних умов являється безбарвним газом. Він без смаку й запаху, мало розчинний в воді, так в 100 об’ємах води за 20°С розчиняється прилизно 3 об’єми кисню. У кисню густина— 1,43 г/л.
За температури -183°С кисень переходить в рідкий стан, за - 219°С – у сині кристали.

Рис. Посудини Дьюара.
Кисень зберігають в спеціальних посуцинах із подвійними стінками, поміж якими відсутнє повітря, які називають посудини Дьюара. Крізь такі стінки дуже повільно теплота передасться у середину посудини, й зріджений кисень, таким чином, випаровується повільно.
Оксиген – це найпоширеніший елемент на планеті. Міститься він у атмосфері, гідросфері, літосфері й навіть живих організмах.
Оксиген формує двохатомні молекули кисню О2.
Кисень являється життєво важливою речовиною. За стандартних умов являє він собою газ без кольору, запаху й смаку, він мало розчинний в воді та трохи важчий за повітря.



Коментарі ( 0 )
Залишити коментар