Конспект уроку: Основні положення молекулярно-кінетичної теорії будови речовини та її дослідні обґрунтування
Навчальна мета: ознайомити учнів з основними положеннями молекулярно-кінетичної теорії будови речовини й їх дослідним обґрунтуванням.
Розділ фізики, в якому вивчаються будова, фізичні властивості та агрегатні стани речовини залежно від їх мікроскопічної структури, називається молекулярною фізикою.
Основними завданнями молекулярної фізики є дослідження:
• агрегатних станів речовини (газів, рідин, твердих тіл), а також умов переходу з одного агрегатного стану в інший;
• будови речовин та змін у їх будові внаслідок зовнішніх впливів (тиску, температури тощо);
• явищ переносу (дифузія, теплопровідність);
• поверхневих явищ на межі розділу середовищ.
Теоретичною основою молекулярної фізики є молекулярно-кінетична теорія речовини (МКТ). Молекулярно-кінетична теорія базується на модельних уявленнях про внутрішню структуру макроскопічних тіл (таких, що складаються з великої кількості частинок), про характер руху і взаємодію частинок у цих тілах. У молекулярно-кінетичній теорії властивості макроскопічних тіл розглядаються як прояв сумарного руху і взаємодії частинок, з яких ці тіла складаються. Отже, розгляд макроскопічних тіл з точки зору МКТ вимагає застосування відповідних методів дослідження.
Очевидно, що механічний (або динамічний) метод, за допомогою якого вивчають рух одного або невеликої кількості тіл, не може бути застосований для дослідження макроскопічних тіл з дуже великою кількістю частинок. Тому молекулярно-кінетична теорія використовує статистичний метод, який дає змогу отримати інформацію не про окремі частинки, а про сукупність їх у цілому. Зазначимо, що за допомогою цього методу розраховуються середні значення фізичних величин, які характеризують рух всіх частинок (середня швидкість руху частинок, середня кінетична енергія поступального руху частинок тощо).
В основі молекулярно-кінетичної теорії лежать три положення, які повністю підтверджені експериментально і теоретично:
1. Всі тіла складаються з частинок - атомів, молекул, іонів.
2. Атоми, молекули та іони перебувають у неперервному хаотичному (тепловому) русі.
3. Між частинками будь-якого тіла існують сили взаємного притягання і відштовхування.
Ці вихідні положення підтверджуються явищами дифузії, броунівського руху, особливостями будови та властивостями рідин і твердих тіл.
Броунівським рухом називають безперервний хаотичний рух дрібних частинок, вміщених у рідину або газ в такі умови, що сила тяжіння не впливає на їх рух (завислі частинки).
Це явище було відкрито у 1827 р. англійським ботаніком Робертом Броуном, який за допомогою мікроскопа спостерігав розчин квіткового пилку у воді. Незабаром виявилося, що подібний рух здійснюють будь-які частинки достатньо малих лінійних розмірів (порядку 10_6 м), але природа броунівського руху протягом тривалого часу не була з’ясованою. Численні спроби пояснити рух частинок як результат дії інтенсивного освітлення, конвекційних потоків рідини, хімічних процесів та інших зовнішніх причин не підтверджувались на дослідах. Було також встановлено, що броунівський рух - не припиняється навіть при довготривалому зберіганні препаратів. Стало очевидно, що пояснити броунівський рух можна лише внутрішніми причинами.
Так, протягом другої половини XIX ст. неодноразово робились спроби зв’язати броунівський рух з тепловим рухом атомів середовища. Але лише у 1905 - 1909 рр. в результаті досліджень Альберта Ейнштейна, Жана Батиста Перрена, Маріана Смолуховського було остаточно встановлено, що броунівський рух є одним з проявів теплового руху атомів і молекул речовини.
Причиною броунівського руху є імпульси, з якими молекули рідини (газу) з усіх боків діють на завислі частинки. Оскільки рух молекул середовища є хаотичним, броунівська частинка у будь-які моменти часу зазнає незрівноважених впливів, що безперервно змінюються за величиною та напрямком. В результаті цього частинка безладно рухається по відрізках складної ламаної лінії.
Пояснення броунівського руху мало принципове значення, оскільки рух атомів і молекул безпосередньо не спостерігається. До того ж, наприкінці XIX та на початку XX ст. деякі вчені скептично відносились до молекулярно-кінетичної теорії речовини - виникали сумніви навіть у реальності атомів і молекул.
Деяке уявлення про характер броунівського руху дає рисунок, одержаний у дослідах Ж. Перрена. Спостереження проводились над частинками гумігута у воді при збільшенні приблизно 3000 разів.
Гумігут - згущений сік жовтого кольору, який збирається з надрізів у стволах деяких тропічних дерев.
Рис. 1. Траєкторія руху Броунівської частинки
Значна інформація про характер броунівського руху та його закономірності держується за допомогою метода, який полягає у макрофотографуванні освітленої завислої частинки протягом тривалого часу. Цей метод забезпечує кількісну перевірку теорії броунівського руху.
З’ясуємо основні закономірності броунівського руху:
•він продовжується необмежено довго без яких-небудь суттєвих змін;
• інтенсивність броунівського руху не залежить від речовини частинок, а залежить лише від лінійних розмірів частинок та їх геометричної форми;
• інтенсивність броунівського руху збільшується із зростанням температури та зменшенням в’язкості рідини (газу).
Отже, броунівський рух є експериментальним підтвердженням існування молекул рідини (газу) та хаотичного характеру їх теплового руху.
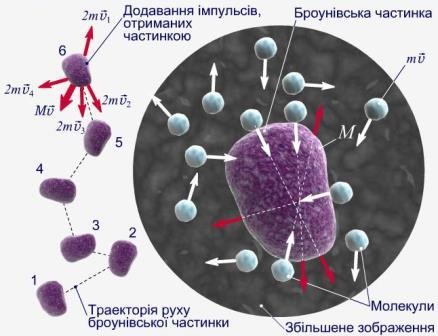
Рис. Хаотичний рух елементарної частинки (положення 1-6) супроводжується змінами напряму і швидкості руху внаслідок постійного бомбардування молекулами газу або рідини, що оточують частинку.
Дифузією називається явище взаємного проникнення різних речовин при їх дотиканні (або змішуванні). Дифузія є результатом теплового руху частинок речовини.
До дифузії здатні атоми, молекули, іони, а також більш великі частинки, які спостерігаються у мікроскоп та приймають участь у броунівському русі. Дифузія має місце у газах, рідинах і твердих тілах.
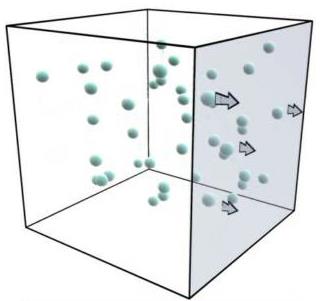
Найбільша швидкість протікання дифузії у газах. Якщо б дифузія у газах визначалась лише швидкістю теплового руху молекул (сотні метрів за секунду), то вона протікала б майже миттєво. Разом з тим, поширення одного газу в іншому відбувається протягом певного часу. Це пояснюється тим, що молекули газів переміщуються між двома точками не прямолінійно, а зигзагоподібно (внаслідок взаємодій з іншими молекулами), що значно збільшує їх шлях між цими точками. Тому швидкість дифузії у газах визначається не лише швидкістю теплового руху молекул, а й довжиною переміщень, які молекули проходять без співударів. Найпростішим прикладом д и фузії у газах є швидке поширення запахів у повітрі.
Дифузія у рідинах відбувається значно повільніше, ніж у газах. Це пов'язане з тим, що молекули у рідинах знаходяться на малих порівняно з газами відстанях, тому дифундуюча частинка протягом деякого часу виривається з оточення найближчих частинок, після чого стрибком переходить в інше положення.
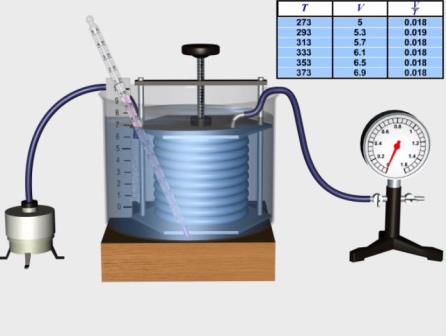
Особливо повільно протікає дифузія у твердих тілах. Якщо з’єднати відшліфовані зразки двох різних металів, наприклад міді та цинку, то за умов найбільшого контакту (під великим тиском) при кімнатній температурі дифузія буде продовжуватись протягом декількох років. Однак, при температурі 100°С - 200°С вже через 12 годин у місті контакту зразків утвориться твердий шар товщиною приблизно 0,25 мм. Це відбувається за рахунок взаємного проникнення частинок, з яких утворені метали, через поверхню розділу внаслідок дифузії. При цьому зразки металу будуть спаяними. Існування дифузії у твердих тілах свідчить про те, що частинки твердих тіл можуть зміщуватись зі своїх положень у вузлах кристалічної решітки.
Наведені приклади показують, що інтенсивність процесу дифузії залежить від температури, оскільки із збільшенням температури зростають швидкості теплового руху молекул.
Дифузія має велике практичне значення у технологічних процесах, оскільки саме дифузією визначається швидкість утворення розчинів, а також протікання багатьох хімічних реакцій. У біологічних процесах з дифузією пов’язана проникність клітинних оболонок.




Коментарі ( 0 )
Залишити коментар