Конспект уроку: Маса та розміри атомів і молекул. Кількість речовини
Навчальна мета: познайомити учнів з поняттями маси й розмірів атомів й молекул;
Розвиваюча мета: навчити школярів визначати кількість речовини.
З’ясуємо основні поняття та означення, якими ми будемо користуватись при вивченні молекулярної фізики.
Атомом називається найменша частинка даного хімічного елемента. Кожному хімічному елементу відповідають певні атоми, які зберігають всі його хімічні властивості.
Молекула - це найменша частинка даної речовини, яка зберігає всі її хімічні властивості і складається з атомів, сполучених між собою хімічними зв’язками.
Маси атомів і молекул у молекулярній фізиці характеризують неабсолютними величинами, а відносними безрозмірними величинами, які називають відповідно відносною атомною Аг та відносною молекулярною Мг масами.
За одиницю атомної маси приймається 1/12 маси атома вуглецю С:
1а.о.м. = 1,66-10-27 кг.
Відносна атомна або молекулярна маси визначаються так:
Відносні атомні маси елементів подаються в періодичній таблиці Менделєєва. Для практичних обчислень відносні атомні маси округлюють до цілого числа.
Одиницею кількості речовини у молекулярній фізиці є моль. Маса не є мірою кількості речовини.
Моль дорівнює кількості речовини, яка містить стільки ж молекул (атомів, іонів), скільки атомів міститься у вуглеці масою 0,012 кг.
З означення випливає, що моль довільної речовини містить однакову кількість молекул (атомів, іонів). Цю кількість називають числом Авогадро на честь італійського вченого XIX ст. Амадео Авогадро:
Масу одного моля називають молярною масою:
Одиницею молярної маси є:
Об'єм одного моля називають молярним об'ємом VM:
де ρ - густина речовини.
Одиницею молярного об'єму є
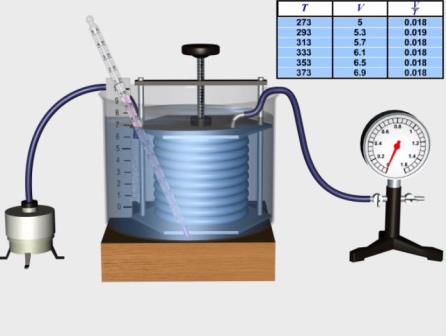
Сучасні методи вимірювання забезпечують досить точне визначення лінійних розмірів частинок речовини, які приблизно становлять у простих атомів і молекул -10-10 м, у складних - набагато більше, наприклад 43-10 м у молекули білка. Сучасна фізика досліджує об'єкти надзвичайно малих розмірів за допомогою електронного мікроскопа, який дозволяє сфотографувати великі молекули.
На рисунках ми будемо зображати молекули у вигляді кульок, проте молекули (атоми) різних речовин мають різну будову і часто дуже складну.
Атоми не мають чітких границь, тому для їх характеристики використовують уяву про атомні радіуси, які дають можливість приблизно оцінити міжатомні відстані у молекулах.










Коментарі ( 0 )
Залишити коментар